喵呜
振动
刚体的转动
功和能
动量与角动量
运动和力
质点运动学
大学物理概述
多元函数的偏导数、全微分与方向导数
多元函数的偏导数
定义:设多元函数 $u=f(\textbf{x})=f(x_1,x_2,\cdots,x_n)$ 在 $\textbf{x}_0=(x_0^{(1)},x_0^{(2)},\cdots,x_0^{(n)})\in \mathbb{R}^n$ 的某个邻域中有定义,若极限
$$\lim_{\Delta x_i\rightarrow0} \frac{\Delta_{x_i}u}{\Delta x_i}=\lim_{\Delta x_i\rightarrow0} \frac{f(x_0^{(1)},\cdots,x_0^{(i-1)},x_0^{(i)}+\Delta x,x_0^{(i+1)},\cdots,x_0^{(n)})-f( \textbf{x}_0)}{\Delta x_i}$$
存在,则称之为$f(\textbf{x})$在 $\textbf{x}_0$ 关于 $x_i$ 的 偏导数,记作 $\frac{\partial f}{\partial x_i}(\textbf{x}_0)$,$\frac{\partial u}{\partial x_i}(\textbf{x}_0)$,$u’_{x_i}(\textbf{x}_0)$ 或 $f’_{x_i}(\textbf{x}_0)$ .
实际上 ,多元函数 $f(\textbf{x})$在 $\textbf{x}_0$ 关于 $x_i$ 的偏导数就是把其他所有变量在这一点固定住,令 $g(x)=f(x_0^{(1)},\cdots,x_0^{(i-1)},x,x_0^{(i+1)},\cdots,x_0^{(n)})$,然后求 $g’(x_0^{(i)})$ 的过程.
例1. 对于二元函数 $f(x,y)=x^2+y^2+xy-x$,求 $\frac{\partial f}{\partial x}(1,1)$ 和 $\frac{\partial f}{\partial x}$.
解:对于 $\frac{\partial f}{\partial x}(1,1)$,我们可以把 $y$ 视为常数 $1$,即 $g(x)=f(x,1)=x^2+1$,$\frac{\partial f}{\partial x}(1,1)=g’(1)=2$.
对于 $\frac{\partial f}{\partial x}$ ,我们还是将 $y$ 视为一个常数. 那么 $g(x)=f(x,y)=x^2+x(y-1)+y^2$,$\frac{\partial f}{\partial x}=g’(x)=2x+y-1$.
烯烃
烯烃的结构、命名和物性
烯烃的结构
由 $\ce{sp^2}$ 杂化轨道形成 $\sigma$ 键、由 $\ce{p}$ 轨道形成 $\pi$ 键组成烯烃分子中的碳碳双键 $\ce{C=C}$.
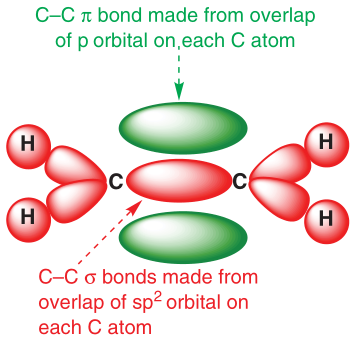
(上图源自Organic Chemistry, p142)
碳碳双键不可旋转、键角为 $120°$、键长小于碳碳单键. 由于 $\pi$ 键电子云重叠程度小,因此 $\pi$ 键不如 $\sigma$ 键稳定,容易断裂,化学反应性较强.
烯烃的同分异构现象
构造异构
对于分子式为 $\ce{C5H10}$ 的烯烃有五个构造异构体: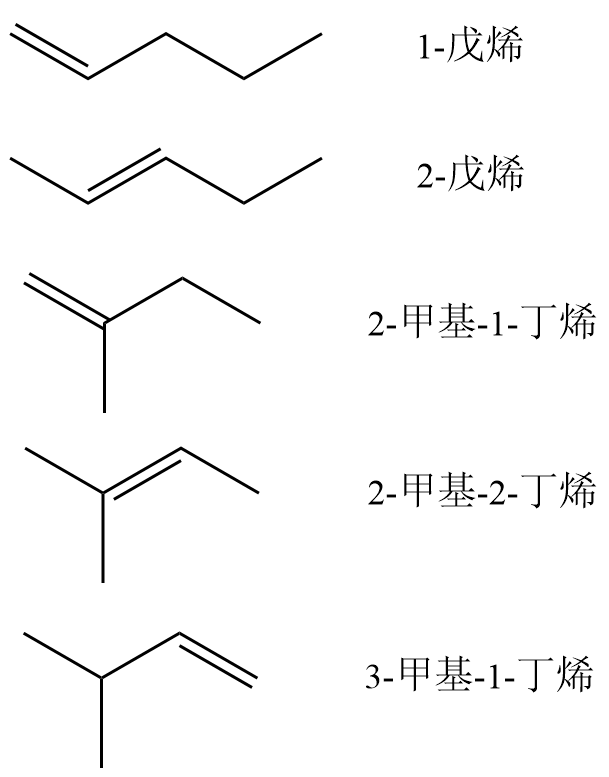
可以看出,有双键位置的异构和碳链的异构两种.
顺反异构
由于碳碳双键不能旋转,因此在碳碳双键的碳原子上各连有两个不相同的基团时,在空间中就会形成不同的排列方式,形成顺反异构体.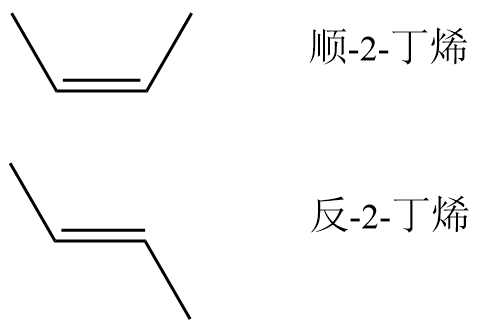
烯烃的命名
常规烯烃的命名
- 选择含有双键的最长链为母体;
- 给双键以最小的编号;
- 指出双键的位置(编号),多于一个双键时,分别用二烯、三烯表示双键个数;
- 对于环状烯烃,编号从双键开始,并沿双键通过,从而使得双键编号最小.
下面给出几个命名实例:
//待绘制
描述烯烃的空间构型(Z,E命名法)
先确定双键相连基团的相对大小,如果大基团在同侧,则为Z构型;反之则为E构型.
下面给出几个命名实例:
待绘制
物理性质
熔点
- 常温下,含2
4个碳原子的烯烃为气体,含515个碳原子的烯烃为液体,高级烯烃为固体; - 通常E型异构体比Z型异构体稳定,并且有较高的熔点;
- 受热时,顺反异构体可以通过 $\pi$ 键的断裂相互转化.
烯烃的化学反应
碳碳双键($\ce{C=C}$)是烯烃的官能团.
与烷烃相比,烯烃的特征反应发生在双键(加成反应)和$\alpha - \ce{C}$上的氢原子(取代反应).
加成反应
在化学反应中,$\pi$ 键断裂,并在原来 $\pi$ 键的两个原子上各连一个原子或基团的反应称作 加成反应.
亲电试剂:试剂在进攻反应中心时,试剂的正电部分较活泼,总是先加在反应中心电子云密度大的原子上.
我们先考察这里 $\pi$ 键的性质.
//例图
由图可知,$\pi$ 键中的电子是裸露的,容易受到亲电试剂的攻击.
与氢卤酸的加成
该反应通式如下:
$$\ce{CH2=CH2 + HX -> CH3CH2X}$$
其中 $\ce{X}=\ce{Cl,Br,I}$.
因为
该反应的机理是 碳正离子中间体机理. 具体表述如下:
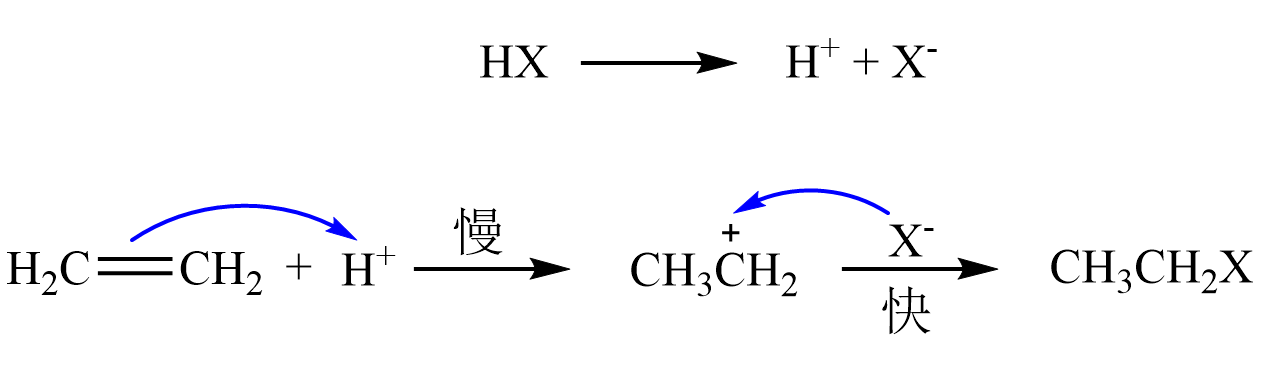
观察第一步(决速步),我们可以了解到,如果氢卤酸的酸性越强($\ce{H+}$越多),反应越容易进行. 因此氢卤酸的反应活性为 $\ce{HI > HBr > HCl}$.
下面我们考虑不对称烯烃的氢卤酸加成.
由实验结果得知,丙烯对氢卤酸的加成产物结果如下:
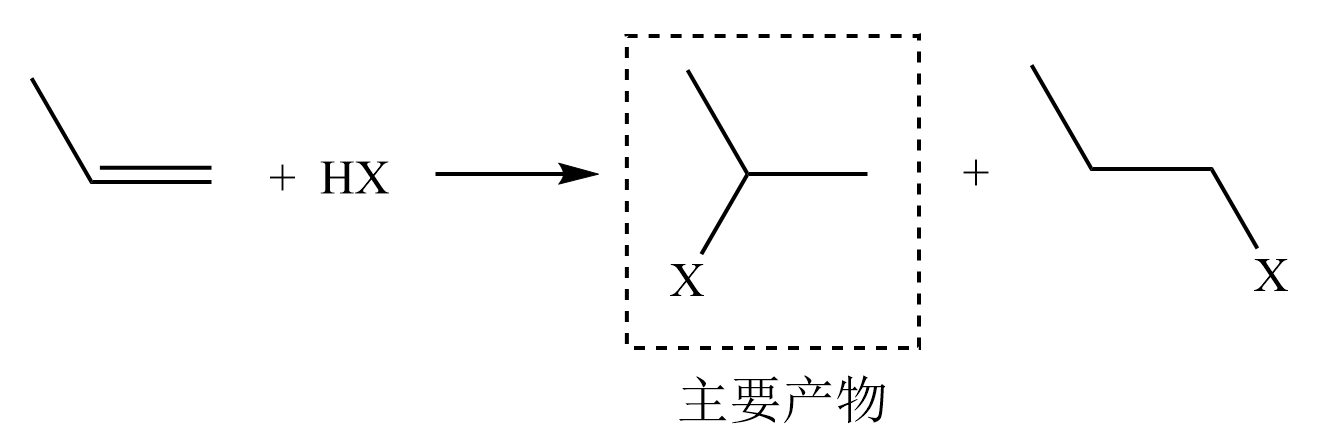
当一个反应可以产生不同异构体时,若反应后主要生成其中一种产物,则称此反应有 区域选择性.
Markovnikov规则:卤化氢等极性试剂与不对称烯烃发生亲电加成反应时,酸中的氢原子加在含氢较多的双键碳原子上,其他原子及基团加在含氢较少的双键碳原子上.
可以从上图发现,烯烃与氢卤酸的加成也有区域选择性,且符合Markovnikov规则.
下面我们用 诱导效应 和 超共轭效应 来解释Markovnikov规则.
诱导效应
诱导效应:因某一原子或基团的电负性而引起电子云沿着键链向某一方移动的效应.
推电子(+I效应):$\ce{R}$基团. $\ce{R3C- > R2CH- > RCH2- > CH3- > H}$.
吸电子(-I效应):由电负性决定. $\ce{-F > -Cl > -Br > -I}$,$\ce{-F > -OH > -NH2}$.
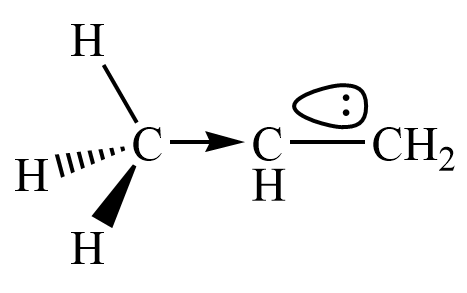
因此对于丙烯,由甲基的推电子效应,$\pi$ 键上电子云向尾端的 $\ce{=CH2}$的碳上偏移. 而又由亲电试剂的正电部分较活泼,总是先加在反应中心电子云密度大的原子上. 因此 $\ce{H+}$ 会先和尾端的 $\ce{=CH2}$ 结合,尾部形成甲基,位于中间的碳上带有一个正电荷.
而后,$\ce{X-}$再与中间的碳正离子结合,生成符合Markovnikov规则的异构体.
超共轭效应
超共轭效应:
碳正离子稳定性:
- 苄基碳正离子>叔碳正离子>仲碳正离子>伯碳正离子>甲基碳正离子
- 平面碳正离子>立体碳正离子
因此对于丙烯,由于仲碳正离子更稳定,因此 $\ce{H+}$ 会与尾端的 $\ce{=CH2}$ 结合,形成仲碳正离子. 也可以理解为,两种离子都会生成,但是伯碳正离子会变为仲碳正离子.
一些氢卤酸加成的实例
1,2-甲基迁移
考虑3,3-二甲基环己烯的加成:
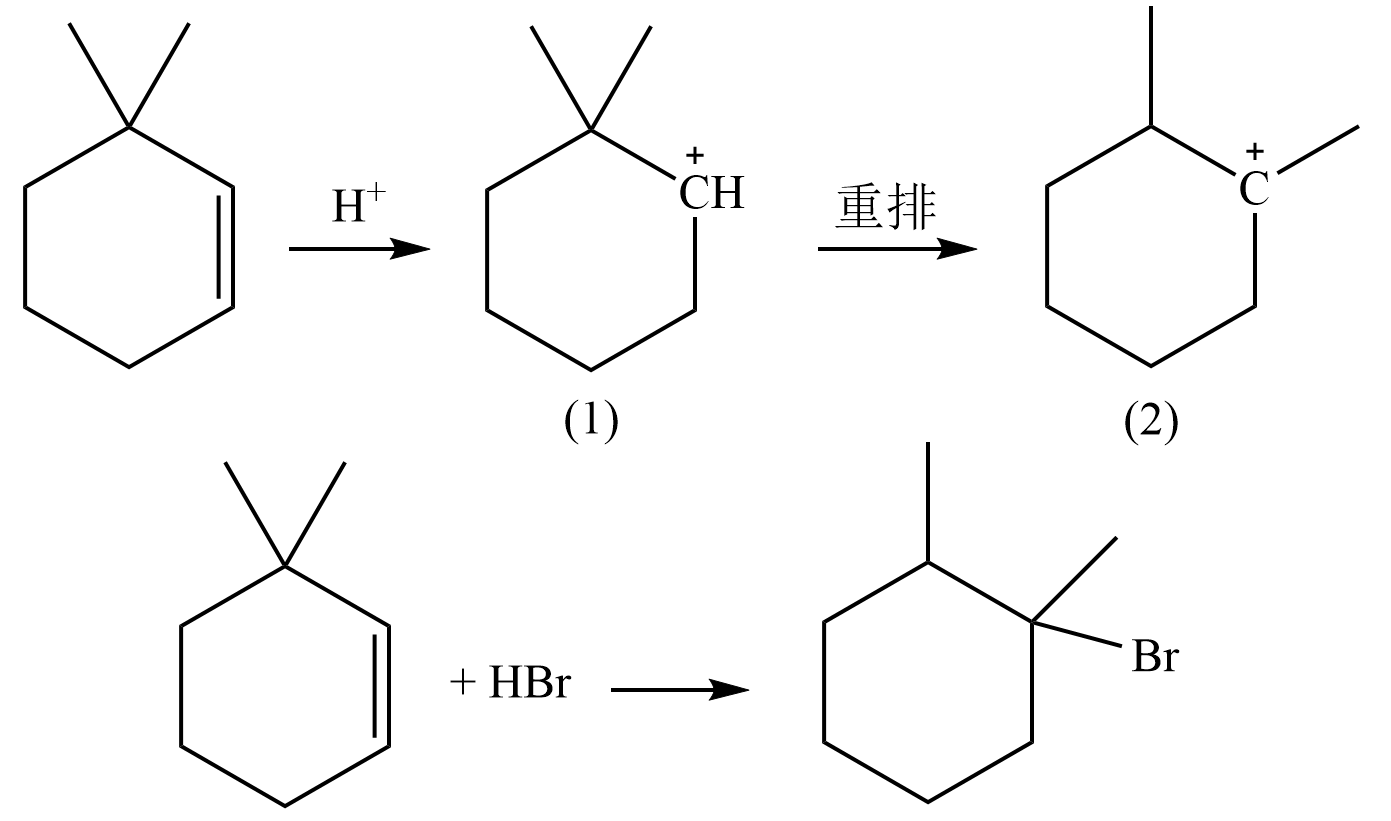
由于稳定性:叔碳正离子>仲碳正离子,因此会发生 $(1)\rightarrow (2)$ 的重排.
1,2-氢迁移
考虑3-甲基-1-丁烯的加成
一些反Markovnikov加成
//苄基
//3,3,3-三氟丙烯
有机合成上的应用
例1. 制备2-氯戊烷.
例2. 制备
与水、醇和有机酸的加成
烯烃与水、醇和有机酸的可以在酸性条件下发生加成反应,反应机理也为 碳正离子中间体机理.
//例图
与水加成时,要用酸催化,先生成碳正离子,然后与水结合形成氧鎓,再失去质子形成醇.
鎓:
与卤素的加成
该反应的通式为:
溴的加成
烯烃与溴的加成是亲电加成,反应机理为 环鎓离子中间体机理,可表述如下:
//例图
*氯与1-苯基丙烯的加成
大多数情况下,氯与烯烃的加成反应也是 环鎓离子中间体机理,但氯与1-苯基丙烯是个例外.
与次卤酸的加成
反应机理也为 环鎓离子中间体机理.
硼氢化反应
乙硼烷的介绍
乙硼烷为气体,无色,有毒,在空气中能自燃. 乙硼烷有两个三中心两电子键,结构如下:
//例图
乙硼烷可以由以下反应制得:
$$\ce{4BF3 + 3NaBH4 -> 2B2H6 + 3NaBF4}$$
烯烃的硼氢化反应
化学方程式:
反应机理:
烷基硼的氧化反应
*烷基硼的还原反应
烯烃亲电加成反应小结
在过氧化物条件下与HBr反应
反应式:
//
发现得到反Markovnikov加成的产物. 这个反应为自由基反应,机理如下:
//
催化加氢
化学方程式:
//
反应发生在金属的表面,是顺式加成.
反应机理:
//
在醋酸汞条件下的水合、还原反应
环氧烷的形成
反应机理
环氧化合物的反应
卡宾(Carbene)加成
卡宾的定义与结构
卡宾的制备
卡宾与碳碳双键的反应
氧化反应
形成邻二醇
烯烃的臭氧化解反应
烯烃的氧化断裂
$\alpha -\ce{H}$ 的反应
$\alpha -\ce{C}$原子:和官能团直接相连的碳原子.
$\alpha -\ce{H}$原子:$\alpha -\ce{C}$上的氢原子.
//例图
在烯烃分子中,$\alpha -\ce{H}$ 受双键的影响,较活泼,可发生卤代反应和氧化反应:
//例图
$\alpha -\ce{H}$ 的卤代反应为自由基反应,机理如下:
//例图